Impf- und therapeutische Wirkstoffe werden heute vielfach mithilfe biotechnologischer Verfahren produziert. Das bedeutet aber auch, dass den biologisch kontaminierten Abwässern aus diesen Prozessen erhöhte Aufmerksamkeit geschenkt werden muss. Welche Wege in der Dekontamination heute beschritten werden und welche Vorteile Systeme bieten, bei denen alle Schritte von der Reinstwassererzeugung bis zur Abwasserentsorgung in einer Hand liegen, stellt der folgende Beitrag vor.
Helmut Sommer
Je nach Biosicherheitsklassen (BL 1, BL 2 oder BL 3) müssen alle Abwässer einer Biotechnologieanlage so aufbereitet werden, dass keine Mikroorganismen in die Werksabwasseranlage gelangen. Diese Dekontamination des Abwassers erfolgt in der Regel über ein Batch- oder über ein kontinuierliches Sterilisationssystem. Das Abwasser stellt häufig eine Mischung aus Gärrückständen, belastet mit entsprechenden Mikroorganismen, Spül- und CIP-Abwässern dar, die auch noch stark variieren und Partikel enthalten können. Deshalb müssen derartige Anlagen sehr robust, aber auch äußerst sicher konzipiert werden. Die Behandlung der biologischen Abwässer stellt somit eine Schlüsselfunktion in der biotechnologischen Produktionsanlage dar.
Die Haupteigenschaften einer Dekontaminationsanlage sind:
- jederzeit 100-prozentig steriles Abwasser
- validierter und dokumentierter Prozess
- Rund-um-die-Uhr-Betrieb möglich
- kurze Chargenzeiten
- geräuscharmer Betrieb
- minimale Unterhaltungskosten
- wartungsarmer Betrieb
Diese Eigenschaften erfüllen sowohl Batch- als auch kontinuierliche Systeme gleichermaßen. Darüber hinaus erlauben Batch-Systeme auch eine einwandfreie Dokumentierung jeder Charge. Der sterile Zustand jeder Abwassercharge kann dabei mithilfe der Prozesssteuerung und der Entnahme von Proben kontrolliert und dokumentiert werden. Um den Dauerbetrieb und eine hohe Durchlaufleistung zu garantieren, lassen sich Chargenbetriebsysteme auch als Doppelanlagen für den Parallelbetrieb konzipieren, so dass immer eine Anlage sterilisiert, während die zweite im Abkühlmodus arbeitet.
Kontinuierliche Anlagen haben dagegen einen wesentlichen Vorteil bei den Betriebskosten, da eine Wärmerückgewinnung zwischen Aufheiz- und Abkühlstrecke möglich ist. Weil bei ihnen jedoch eine eindeutige Zuordnung der Chargen nicht gewährleistet ist, werden diese Anlagen in der Regel nur für schwach kontaminierte Abwässer eingesetzt.
Anwenderorientiert von A bis Z für reibungslosen Betrieb
Um den unterschiedlichen Nutzerbedürfnissen gerecht zu werden, sollten Dekontaminationsanlagen modular aufgebaut und individuell geplant sein. Grundsätzlich gilt hier wie immer in den sensiblen pharma- und biotechnologischen Bereichen: Je weniger Schnittstellen bei Planung und Bau der Anlagen nötig sind, desto sicherer arbeitet das System. Gesamtsysteme, die die Reinstwasser- und Reinstdampfversorgung mit kompletten Prozesslösungen wie der Abwasserbehandlung kombinieren, gewährleisten höchstmögliche Sicherheit. So entsteht nach dem Turnkey-Konzept eine komplette pharmazeutische Fertigung aus einer Hand. Das bedeutet: rasche und schnittstellenreduzierte Projektabwicklung, integrierte Steuerungssysteme mit PLC-Steuerung, die einen wartungsfreien und vollautomatischen Betrieb ermöglichen, sowie eine einheitliche, vollständige Dokumentation der gesamten, GMP-konform gefertigten Anlage. Auch Ausführungen mit Erfüllung der Dokumentationsschritte gemäß 21 CFR Part 11 sind hier problemlos integrierbar.
Verfahrenstechnischer Aufbau des Batch-Verfahrens
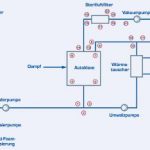
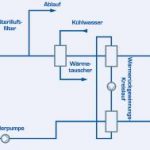
Beim Batch-Verfahren wird das Abwasser in einem Puffertank gesammelt. Je nach Füllstand des Tanks wird es mit Pumpen in den Sterilisationsautoklaven gefördert. Gesättigter Dampf heizt das Abwasser hier auf und sterilisiert es bei Temperaturen von mehr als 121,1 °C. Die Konstruktion und Platzierung der Dampfzufuhr ist kritisch für die gesamte Prozessabwicklung sowie den Geräuschpegel des Verfahrens. Um eine Geräuschreduktion, eine hohe Zuverlässigkeit und die gleichmäßige Aufheizung der Gesamtanlage zu erreichen, sollte diese mit einem Vakuumsystem ausgestattet sein. Dabei wird die Autoklavenkammer vor dem Sterilisationsprozess mithilfe einer Vakuumpumpe evakuiert. Während der Sterilisation ist dadurch gewährleistet, dass die gewünschte Temperatur alle Oberflächen im Autoklaven sowie in den Abluftkanälen zuverlässig erreicht. So werden auch dort festgesetzte Mikroorganismen endgültig zerstört. Eine einwandfreie Sterilisation, bei der die Temperatur üblicherweise zwischen 125 und 135 °C liegt, ist aus diesem Grund garantiert. Der Prozess ist dann erfolgreich abgeschlossen, wenn diese Temperatur über mindestens 30 Minuten an allen Stellen eingehalten wurde. Alle Sterilisationsparameter sind dabei frei konfigurierbar, Veränderungen werden entsprechend dokumentiert und im Prozess registriert.
Einen weiteren kritischen Punkt derartiger Anlagen stellt die erwähnte Behandlung der Abluft der Autoklavenkammer dar. Sie kann zu Geruchsbelästigung führen und darüber hinaus mit Mikroorganismen kontaminiert sein. Die Abluftbehandlung erfolgt in modernen Anlagen deshalb in zwei Schritten. Zunächst werden die Mikroorganismen durch eine Sterilfiltration zurückgehalten; im Anschluss sorgt eine Desodorierung für die Beseitigung eventueller Gerüche. Sterilfilter sowie Abluftkanäle werden während jeder Sterilisation ebenfalls erhitzt und damit dekontaminiert und das anfallende Kondensat grundsätzlich in das Puffersystem zurückgeführt, so dass keine nicht sterilen Bestandteile nach außen gelangen können. Nach Abschluss des Prozesses wird das sterile Abwasser mithilfe eines Plattenwärmeaustauschers abgekühlt. Ist eine Temperatur von 40 °C erreicht, entleert sich der sterile Inhalt des Autoklaven automatisch ins Abwassersystem, sofern alle Prozessparameter eingehalten worden sind. Der Autoklav ist somit bereit, den nächsten Prozess automatisch zu starten und zu dokumentieren.
Da einige Abwässer, wenn sie mit Dampf aufgeheizt werden, Schaum bilden, wird in solchen Anwendungsfällen eine Antischaum-Dosierungsanlage in der Saugleitung der Förderpumpe installiert. Aufheiz- und Abkühlzeiten sowie der Einsatz von Vakuumschritten müssen dabei zusätzlich optimiert werden, um auch bei solchen Prozessen den optimalen Energieeinsatz und die maximalen Durchsatzmengen zu erreichen.
Liproline-System folgt Turnkey-Gedanke
Vom Reinstwasser-Spezialisten Christ stehen zur Behandlung von belastetem Abwasser Dekontaminationsanlagen aus der Liproline-Reihe, die auch Mischbehälter, Ansatzlinien und CIP/SIP-Systeme umfasst, zur Verfügung. Diese sind wahlweise als vollautomatisches Batch- oder kontinuierliches Verfahren ausgelegt. Das inaktivierte Abwasser kann über das normale Werks-Abwassernetz entsorgt werden. Optional lässt sich eine Abluftreinigung ergänzen, die Geruchsbelästigungen vermeidet. Mit den Liproline-Systemen für Abwasseraufbereitung wird den Lösungen das Wasser entzogen und das zu entsorgende Material stark reduziert. Darüber hinaus sorgt die spezielle Verdampfertechnologie für eine Inaktivierung bestimmter Wirkstoffe. Je nach Anwendung kann diese auch mit den UV-Geräten der Liproline-Baureihe durch eine kostengünstige UV-Oxidation vorgenommen werden.
Reibungslose Inbetriebnahme spart Zeit und Kosten
Da für Reinstwasser- und Dekontaminationsanlagen die Vorschriften bezüglich biologischer Sicherheit gelten, müssen umfangreiche Installations- und Funktionstests durchgeführt werden. Hierbei sind neben der Einhaltung der Druckbehälterverordnung auch Schweißnahtüberwachungen mit Probenähten, Endoskopie sowie eventuell Röntgenkontrollen erforderlich.
Wie bei allen pharmazeutischen Anlagen steht vor dem Anlagentest eine Installationsqualifizierung mit Überprüfung aller Einzelpunkte von Materialzertifikaten bis hin zu Loopchecks und Alarmmeldungen der SPS. Während des FAT’s (Factory Acceptance Test) wird dann ein Wärmeabbildungstest an speziell festgelegten Stellen der Anlage durchgeführt, um den gesamten Sterilisationsprozess zu validieren. Geprüft wird dabei unter anderem eine Zwangsunterbrechung der Anlage, um aufzuzeigen, dass der Sterilisationsprozess danach wieder korrekt einsetzt. Ein Test der Gesamtanlage unter Volllast bereits beim Hersteller ist notwendig; nur so lassen sich alle späteren Einflüsse des Systems sicher prüfen. Die Gesamtqualifizierung der Abwasseranlage ist wie bei jeder Sterilproduktionsanlage unerlässlich, um den behördlichen Anforderungen gerecht zu werden. Umfangreiche Qualifizierungsunterlagen für IQ und OQ werden von Herstellern wie Christ bereitgestellt und gemeinsam mit dem späteren Anwender im Rahmen des FAT’s schon im Werk geprüft. Bei den späteren Funktionstests vor Ort werden die Anlagen an alle Versorgungssysteme der Produktionsstätte angeschlossen und unter realen Bedingungen getestet und dokumentiert.
Fazit
Systeme zur Sterilisierung des Abwassers in biotechnischen Anlagen sind bereits heute häufig vorgeschrieben beziehungsweise unerlässlich. Vollautomatische, qualifizierte Chargensterilisations- oder kontinuierliche Systeme sorgen für einen zuverlässigen Betrieb und sind je nach Anwendungsfall auf die nutzerspezifischen Bedingungen anzupassen. Dazu sollten sie auf modularen Herstellersystemen wie der Liproline-Reihe von Christ aufbauen, die idealerweise bereits die Reinstwassererzeugung und -verteilung umfassen, denn Sicherheit steht bei derartigen Anwendungen an oberster Stelle.
Halle 4.1, Stand J8
cav 497
Mehr zu Liproline
Internetportal Biotechnologie
Unsere Whitepaper-Empfehlung
Wasserstoff gilt als Schlüssel für die Dekarbonisierung der Chemieindustrie. Doch die Nutzung des vermeintlichen Hoffnungsträgers Hydrogen birgt auch Gefahren und stellt die Branche vor neue Herausforderungen, die das gratis Whitepaper „H2 wie Hoffnungsträger?“ näher für Sie…
Teilen: