Abk.: PTFE.
Zur Untergruppe der Fluorpolymere zählender Polymerwerkstoff.
PTFE als vollfluorierter Kunststoff hat hervorragende thermische und chemische Beständigkeitseigenschaften. Von Nachteil ist, dass PTFE weder kleb- noch schweißbar (Kleben, Schweißen) ist, kaum thermoplastische Verarbeitung (Thermoplaste) zulässt und zudem einen deutlichen Trend zum Kaltfließen unter mechanischer Spannung zeigt. Klebeprobleme ergeben sich aus der sehr geringen Oberflächenenergie von PTFE. Probleme beim Schweißen bzw. bei der thermoplastischen Verarbeitung (Extrudieren, Spritzgießen) ergeben sich aus dem Sachverhalt, dass Schmelztemperatur und thermische Zersetzungstemperatur von PTFE sehr eng beieinander liegen.
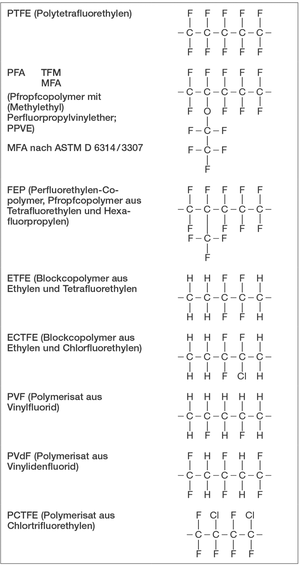
Chemische Weiterentwicklungen des PTFE durch Copolymerisation haben zu sogenannten Isomeren bzw. Derivaten des PTFE geführt: PFA (TFM, MFA), FEP bzw. ETFE, PCTFE bzw. ECTFE. Hierbei handelt es sich im Wesentlichen um eine Reihe von (Pfropf-)Copolymeren, die einerseits die thermoplastische Verarbeitbarkeit bzw. das Verschweißen erlauben, bei denen andererseits aber die chemische und thermische Widerstandsfähigkeit gegenüber PTFE merklich eingeschränkt wird. Auch der Kristallisationsgrad (molekularer Ordnungsgrad) ist v. a. bei Pfropfcopolymeren im Vergleich zu PTFE deutlich geringer; ebenso die Kettenlänge der Makromoleküle.
Die strukturellen Änderungen der PTFE-Copolymere im Vergleich zu PTFE führen zu wesentlichen Eigenschaftsänderungen, so z. B. zu einem deutlich niedrigeren Schmelzbereich. Die Bindungsenergien (Tab. P 5) der Primärbindungen (Chemische Bindungen) innerhalb der Makromoleküle und der Sekundärbindungen zwischen den Makromolekülen geben Hinweise auf den Umfang der Eigenschaftsänderungen der betreffenden Copolymere im Vergleich zu PTFE.
| Primäre Bindungen | Bindungsenergie in kcal/g mol |
| C − C (aliphatisch) | 59,6 |
| C = C | 102,1 |
| C ≡ C | 126,5 |
| C − H | 88,2 |
| C − O | 70,5 |
| C − N | 57,8 |
| C − F | 110 |
| C − CI | 68,6 |
| Si − O | 89,3 |
| Sekundäre Bindungen | |
| − CH3 | 1,78 (Wasserstoff-Brücken) |
| − OH | 7,25 (Wasserstoff-Brücken) |
Abb. P 10: Beispiele für die verschiedenen Derivate von PTFE. (Quelle: G. Henkel)
© 2013 – ECV – Lexikon der Pharmatechnologie