Alljährlich lädt die BASF Journalisten und Wissenschaftler zu einer Gesprächsrunde ein. Thema der letzten Veranstaltung, die im Herbst 1998 stattfand, war „Analytik in der industriellen Chemie“. Es folgen Auszüge aus einem Vortrag von Dr. Manfred Essig, Leiter Mikrostrukturuntersuchungen und Thermoanalytik im Ammoniaklaboratorium der BASF, der sich mit der Analytik in der Katalysatorforschung beschäftigte.
Die meisten heterogenen Katalysatoren wurden in jahrzehntelangen Arbeiten empirisch – durch „trial and error“ – zu Hochleistungssystemen entwickelt. Mit den modernen Methoden der Festkörpercharakterisierung ist es heute möglich, die Beziehungen zwischen der Struktur und den Eigenschaften solcher Systeme aufzuklären und damit den Ablauf heterogen katalysierter Prozesse besser zu verstehen.
Anzeige
Die Überwachung von Pumpen in industriellen Prozessen ist weit mehr als eine reine Schutzmaßnahme für das Pumpenaggregat. Neben der präventiven Wartung und...
Über die allgemeinen analytischen Zielsetzungen hinaus kommt es bei der Analyse funktionaler Festkörper, zu denen auch die Katalysatoren gehören, darauf an die Heterogenität des Festkörpers, also die räumliche Verteilung von Strukturelementen im Nano- oder Mikrometermaßstab, aufzuklären. Diese ist für die Funktionalität entscheidend. Eine Analytik, deren Ziel die Erarbeitung von Struktur-Eigenschaftsbeziehungen ist, muß folglich strukturgetreue Informationen liefern. Bei heterogenen Katalysatoren ist also die Verteilung und Anzahl der funktional bedeutsamen Strukturelemente zu ermitteln.
Charakterisierung und Entwicklung von Katalysatoren
Die Eignung eines Katalysators für eine bestimmte Reaktion in einem chemischen Produktionsprozeß läßt sich nach verschiedenen Kriterien bewerten. Dazu zählen beispielsweise die Aktivität des Katalysators, seine Selektivität und Lebensdauer.
Die äußere Oberfläche der Katalysatorformkörper ist klein gegenüber der katalytisch wirksamen inneren Oberfläche, die schon unmittelbar an und unter der äußeren Oberfläche des Formkörpers zur Verfügung steht. Die für die Moleküle erreichbare Kontaktfläche, die die Aktivität des Katalysators maßgeblich bestimmt, läßt sich durch zwei Maßnahmen vergrößern:
• Um mit wenig Katalysatormasse eine große Oberfläche zu erreichen, werden die katalytisch wirksamen Feststoffe in Form sehr kleiner Teilchen mit einem Durchmesser im nm-Bereich bereitgestellt. Auf diese Weise wird auch der Einsatz von Edelmetallen als katalytisch aktives Material erschwinglich.
• Man sorgt für eine feinporöse Struktur des Katalysators, so daß die inneren Oberflächen über ein feinverästeltes Porensystem untereinander und mit der Oberfläche des Formkörpers in Verbindung stehen.
Zudem ist es sehr wichtig, daß die entstandenen Reaktionsprodukte möglichst schnell von der Katalysatoroberfläche weggeleitet werden.
Im Laufe der Katalysatorentwicklung müssen mit vielfältigen physikalischen Methoden zur Katalysatorcharakterisierung zahlreiche Strukturmerkmale aufgeklärt werden. Dazu gehören: die chemische Zusammensetzung der kleinsten Teilchen oder Phasen, deren innere Struktur, Ausdehnung und Gestalt, außerdem Agglomerationszustände, Vergesellschaftungen, Belegungsdichten, Dichtegradienten usw.
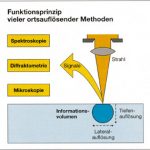
Den physikalischen Meßmethoden zur mikrostrukturellen Untersuchung heterogener Katalysatoren liegt ein gemeinsames Funktionsprinzip zugrunde (Abb. 2): Die Katalysatorprobe wird mit einem Photonen-, Elektronen- oder Ionenstrahl beschossen; diese Strahlung löst dort, wo sie auf die Katalysatorstrukturen auftrifft, ein Signal aus. Die spektroskopische, diffraktometrische oder mikroskopische Signalauswertung liefert anschließend Informationen über die chemische Zusammensetzung, die Strukturen bzw. die Morphologie.
Die einzelnen Untersuchungsmethoden unterscheiden sich im Fokussierungsgrad und in der Energie der anregenden Strahlung. Von der Art und der Energie der Signale hängen die Orts- und Tiefenauflösung der einzelnen Methoden ab. Die von den Signalen gelieferten Informationen stammen allerdings aus einer Tiefe von höchstens einigen zehn Mikrometern; deshalb wurden Präparationstechniken entwickelt, mit denen Katalysatoren „seziert“ werden können. Auf diese Weise lassen sich auch unter der Oberfläche verborgene Strukturen genau analysieren.
Wegen der unterschiedlichen Art und Menge der Informationen liefert aber nur der simultane Einsatz mehrerer Methoden eine verläßliche Katalysatorcharakterisierung. Deshalb müssen die Katalysatorentwickler der BASF gelegentlich den eigenen Instrumentenpark durch Zugriff auf externe Forschungseinrichtungen mit entsprechender Ausstattung ergänzen.
Silberhaltiger Trägerkatalysator für Oxidationsprozesse
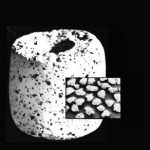
Der Formkörper dieses Katalysators ist eine hochporöse Ringtablette aus Aluminiumoxid, auf die etwa 20 Gewichtsprozent Silber und Spuren eines Promotors, der die Selektivität des Katalysators erhöht, aufgebracht werden. Bereits bei geringer Auflösung sind in der raster-elektronenmikroskopischen Aufnahme (SEM) an der Katalysatoroberfläche die Öffnungen der nach innen führenden Poren zu erkennen (Abb. 3). Bei höherer Auflösung wird sichtbar, daß die Silberteilchen an der Ringmanteloberfläche eines jungen Katalysators kaum ein tausendstel Millimeter groß sind. Bei einem im technischen Reaktor über eine längere Betriebszeit gealterten Katalysator sind die Silberteilchen etwas größer und zeigen Ecken und Kanten, die neu gebildete Kristallflächen begrenzen (Abb. 4).
Daß es sich bei den Teilchen um Silber handelt, beweist die Elektronenstrahl-Mikrobereichsanalyse (EPMA). Dabei wird ein Elektronenstrahl mit fast beliebig wählbarer Fleckgröße auf die zu untersuchende Stelle der Probe gerichtet. Die daraufhin austretende Röntgenstrahlung ist charakteristisch für die dort vorliegenden Elemente. Die Konzentration des Promotorelements liegt unter der Nachweisgrenze dieser Methode.
Um die Verteilung des Silbers im Formkörper zu ermitteln, wird aus seiner Mitte eine Scheibe herausgetrennt. Die EPMA über diese Querschnittsfläche zeigt, daß die Silberkonzentration im Zentrum des Ringmantels geringer ist als außen (Abb. 5). Auch sind die Silberteilchen dort kleiner als an der Außenoberfläche. Diese kleinen Teilchen stellen aber trotz ihrer geringeren Masse eine ungefähr gleich große Oberfläche für die Katalyse zur Verfügung wie die größeren Silberteilchen am Rand. Dieser Befund ist wichtig, weil der Katalysator während seiner Entwicklung im Labor zerkleinert werden muß. Für die Übertragbarkeit der Laborergebnisse auf den Produktionsprozeß muß sichergestellt sein, daß der zerkleinerte Katalysator die gleiche katalytisch wirksame Kontaktfläche hat wie der unversehrte Formkörper.
Auch die Frage, ob die Ausdehnung der Silberoberfläche allein für die Katalysatoreigenschaften verantwortlich ist, muß geklärt werden. Das ist dann zu erwarten, wenn alle Silberteilchen und vor allem auch ihre Oberflächen die gleiche Struktur haben. Die Röntgenbeugung zeigt, daß das Silber kristallin ist. Allerdings liefert diese Methode nur eine pauschale Aussage, da mit ihr die einzelnen mikrometergroßen Teilchen nicht individuell untersucht werden können. Das Beugungsdiagramm zeigt neben den Reflexen des Trägermaterials Aluminiumoxid – harter Korund, der mit Diamantwerkzeugen zur Scheibe präpariert wurde – die Silberreflexe (Abb. 6). Aus der Breite der Reflexe kann die Größe der reflektierenden Silberkristallite bestimmt werden. In unserem Beispiel findet man Werte von 25 nm bzw. 100 nm. Aus der mittleren Größe der Kristallite und der Dichte des Silbers könnte jetzt die Größe der Silberoberfläche abgeschätzt werden.
Doch die Auswertung der elektronenmikroskopischen Aufnahmen zeigt, daß die Teilchen größer sind als die nach dem geschilderten Verfahren ermittelte Kristallitgröße. Worauf ist diese Diskrepanz zurückzuführen?
Durchleuchtet man die Teilchen in einem Transmissions-Elektronenmikroskop (TEM), dessen Elektronenenergie etwa zehnmal so hoch ist wie die Elektronenenergie eines Raster-Elektronenmikroskops, dann wird sichtbar, daß die Silberteilchen aus mehreren Kristalliten bestehen. Sie sind also durchaus nicht homogen und nahtlos aufgebaut, sondern polykristallin. Bei den Nähten handelt es sich um Korngrenzen, und die oben erwähnten Kristallflächen sind nicht die Flächen eines Einkristalls, sondern die Flächen unterschiedlich orientierter Kristallite. Mit der Röntgenbeugung wurde also die Kristallitgröße und nicht die Teilchengröße bestimmt.
Die klassische Methode zur Bestimmung einer Metalloberfläche ist die Chemisorption. Bei ihr wird die Bedeckung der Metalloberfläche mit Sondenmolekülen ausgewertet. Leider versagt diese Methode bei der Bestimmung der Silberoberfläche aus Mangel an geeigneten Sondenmolekülen und wegen der hohen Löslichkeit von Sauerstoff in Silber. Hier hilft nur die Auswertung der mikroskopischen Abbildungen der Silberteilchen mit der digitalen Bildanalyse weiter, mit der die mittlere Teilchengröße und sogar die Teilchengrößenverteilung ermittelt werden können. Dieser Weg ist allerdings aufwendig, da die Bearbeitungsschritte manuelles Eingreifen erfordern.
Aus dem Verhältnis von mittlerer Teilchengröße zu mittlerer Kristallitgröße läßt sich die Zahl der Kristallite und damit auch die Häufigkeit von Korngrenzen in einem Silberteilchen abschätzen. Für die Katalysatoreigenschaften sind nicht nur bestimmte Kristallfacetten an der Oberfläche relevant, sondern auch Korngrenzen, in denen die atomare Ordnung erheblich gestört ist. Diese Bereiche spielen bei diesen Oxidationskatalysatoren eine wichtige Rolle für den Transport von molekularem und atomarem Sauerstoff und für den Sauerstoffhaushalt im Silber. An diesen Grenzen hält sich wahrscheinlich auch das Promotorelement auf und steuert als Strukturpromotor die Ausbildung und Stabilisierung der Korngrenzen. Sein analytischer Nachweis scheitert allerdings noch an den Grenzen der Ortsauflösung und an der Empfindlichkeit der Meßmethoden.
Vollkatalysator für die Oxidation von Kohlenwasserstoffen
Mehrere oxidische, katalytisch aktive Phasen charakterisieren diesen Vollkatalysator für die Oxidation von Kohlenwasserstoffen. Hier liegt der Katalysatorentwicklung die Vorstellung zugrunde, daß bestimmte Festkörperphasen den Sauerstoff aus dem Gasraum aufnehmen, er jedoch von einer anderen Phase an das Zielmolekül abgegeben wird. Die heterogene Struktur des Katalysators bestimmt also seine Funktionalität.
Mit der Abbildung der Verteilung eines Elements im Querschnitt des Formkörpers kann die Verteilung einer mehratomigen Katalysatorphase dargestellt werden, wenn das gewählte Element für die Phase repräsentativ ist. Im genannten Beispiel verändert sich die kupferreiche Phase während der Betriebszeit des Katalysators auffällig: Sie grenzt sich aus einem hochdispersen Anfangszustand zu räumlich wohl definierten Bereichen gegenüber den anderen Katalysatorphasen ab. Anfangs verbessert sich parallel dazu die Selektivität des Katalysators.
Zunächst mußte die Struktur dieser Phase identifiziert werden. Nur wenige mikrometergroße Bereiche des am längsten gealterten Materials wurden dazu so präpariert, daß mit einer fokussierbaren und mikroskopisch positionierbaren Röntgenbeugungseinrichtung das Röntgenbeugungsdiagramm aufgenommen werden konnte. Doch obwohl die stöchiometrische Zusammensetzung bekannt war, konnte das Material anhand dieses Beugungsdiagramms in keiner Datenbank gefunden werden. Nach zahlreichen Präparationsversuchen gelang es, größere Mengen des Materials in Pulverform herzustellen. An diesem wurde anschließend eine Strukturaufklärung durchgeführt: Durch Nutzung einer modernen Software für die Strukturaufklärung sowie einer Molecular-Modeling-Software und unter Einsatz der Elektronenbeugung im Transmissions-Elektronenmikroskop gelang schließlich die Aufklärung der Struktur des Materials. Es handelte sich um ein Kupfermolybdat.
Weitere Informationen cav-282
Unsere Webinar-Empfehlung
Die Websession „Wasserstoff in der Chemie – Anlagen, Komponenten, Dienstleistungen“ (hier als Webcast abrufbar) zeigt technische Lösungen auf, die die Herstellung und Handhabung von Wasserstoff in der chemischen Industrie sicher machen und wirtschaftlich gestalten.
Ob effizienter…
Teilen: