Durch den verstärkten Einsatz von hochaktiven Wirkstoffen werden offene Herstellungsprozesse zukünftig nicht mehr möglich sein oder gar genehmigt werden. Hier bietet die kontinuierliche Herstellungstechnik Vorteile gegenüber der klassischen Chargenproduktion, vor allem bei der Produktion kleinerer Volumina, der Gefährdung des Bedienpersonals und der Reduktion des Produktionsraumes.
Sogenannte Small Molecules oder OSDs (Oral Solid Dosage) machen circa zwei Drittel aller pharmazeutischen Produkte weltweit aus. Dieser Wert bezieht sich dabei allerdings auf die Menge der Produkte und nicht auf die Höhe des Umsatzes. Erfolgreiche Medikamente mit hohem Marktpotenzial, sogenannte Blockbuster, sowie Monoanlagen werden immer weniger, da mehr und mehr Patente großer Blockbuster auslaufen.
In den letzten Jahren wurden pharmazeutische Wirkstoffe produziert, die immer stärker bzw. aktiver in ihrer Wirkung sind. Diese Steigerung der Potenz/Stärke neuer Wirkstoffe erfordert nun ein Umdenken in der Industrie. High-Containment-Anlagen sind erforderlich, um Kreuzkontaminationen zum Schutz des Produktes, der Bediener und der Umwelt (besonders bei der Herstellung von HAPIs (High Potency Active Pharmaceutical Ingredients) zu vermeiden. Kontinuierliche Herstellungsanlagen sind daher hervorragend geeignet, um derartige Produkte herzustellen, da diese keine manuellen Zwischenschritte, beispielsweise das Umfüllen eines Zwischenproduktes in einen IBC von einem Prozessschritt zum nächsten, erfordern und damit das Risiko einer Kreuzkontamination minimieren.
Zudem werden die behördlichen Bestimmungen von EMA, FDA, PICs, EHS, Reach etc. zunehmend restriktiver und stringenter, sodass zusätzliche Methoden, Maschinen und Gebäudevoraussetzungen benötigt werden, die diesen Anforderungen gerecht werden.
Wieviel Containment ist erforderlich?
Der englische Begriff Containment bezeichnet im Allgemeinen die Abschirmung der Umwelt von Belastungen durch Wirk- und Hilfsstoffe. Unter Containment werden alle Maßnahmen eingeschlossen, die eine Ausbreitung hochwirksamer Substanzen begrenzen. Der Umfang des Containments ist dabei immer individuell und relativ zum Produkt. Mit Containment ist keinesfalls immer ein sogenanntes geschlossenes System gemeint. In der Praxis lautet die Frage nicht „Ist ein Containment nötig?“ sondern „Wieviel Containment ist erforderlich?“ Denn: Ein total geschlossenes System gibt es nicht.
Containment umfasst ein weites Anwendungsfeld, in dem bisher keine einheitlichen Regelwerke verfügbar waren. Erst im November des vergangenen Jahres hat die ISPE D/A/CH (International Society for Pharmaceutical Engineering) in Bad Dürkheim auf einem Containment-Seminar das Containment-Handbuch in deutscher Sprache veröffentlicht. Bisweilen ist dieses Buch nur in Deutsch verfügbar, soll aber in absehbarer Zeit ins Englische übersetzt werden. Bereits vier Wochen nach der Vorstellung des Handbuches wurde es von Lieferanten und Anwendern in der Industrie als neues Standardwerk und Referenz benutzt.
Für die Herstellung potenter Stoffe werden in der Regel Containment-Maßnahmen fünf verschiedener Kategorien verwendet (Bild 1), bei denen hauptsächlich das OEL/OEB/CAT-System Anwendung findet (OEL/OEB, Occupational Exposure Limit/Band). Zusätzlich haben sowohl pharmazeutische Großunternehmen als auch Lieferanten eigene Systeme entwickelt, die eigene Kategorisierungen und Grenzen festlegen. Die Verwendung unterschiedlicher Kategorien durch Equipment-Hersteller und Pharmaunternehmen kann daher zu möglichen Unsicherheiten oder falschen Annahmen führen, wenn diese nicht zu Beginn eines Projektes abgeglichen und definiert werden. Zudem muss darauf hingewiesen werden, dass neben Klasse, Band oder Kategorie eines Wirkstoffes auch der OEL-Wert über einen Zeitraum von 8 Stunden (in µg per m3) in die Projektierung eingeschlossen werden muss. Durch die Verwendung des Containment-Handbuches sollte sich in Zukunft eine Vereinheitlichung dieser Kategorien verwirklichen lassen.
Geschlossene Prozesse
Um sich die Menge an Wirkstoff in einem Raum besser vorstellen zu können, soll hier ein Beispiel dienen: Man stelle sich ein olympisches Schwimmbecken mit einer Größe von 50 x 25 x 2 m resultierend in einem Volumen von 2500 m3 vor. Wirft man nun eine Prise Salz, also etwa 2,5 mg oder 25 Salzkörner, in dieses Schwimmbecken, so erhält man eine Konzentration von einem Mikrogramm je Kubikmeter (1 µg/m3), was der höchsten Containment-Stufe entspricht (Bild 2).
Wie bereits erwähnt, stellt sich nicht die Frage, ob sondern wie viel Containment für die Produktion eines potenten Wirkstoffes benötigt wird. Die wachsende Sensibilisierung gegenüber Arbeitsplatzgrenzwerten lässt einen zunehmenden Trend zu geschlossenen Produktionsprozessen besser erkennen, sodass in nicht allzu ferner Zukunft keine offenen Prozesse mehr zugelassen werden, um sowohl den Bediener als auch das Produkt zu schützen.
Geschlossene Prozesse sind allerdings nicht zwangsläufig gleichbedeutend mit einem kompletten Containment-Isolator. Abhängig von der Potenz eines Stoffes kann es bereits ausreichend sein, ein leichtes oder einfacheres Containment in den Produktionsprozess zu integrieren. Beispiele für leichtes Containment sind eine Doppelklappe oder ein geschlossener Behälter, bei dem zur Überführung von Rohstoffen eine geschlossene Leitung benutzt wird. Weiterhin kann eine Tablettenpresse, die geschlossen ist und geschlossen befüllt wird, ein einfaches Containment darstellen. Aber auch integrierte Produkttransferleitungen und Filter, die abreinigbar sind und Abschirmungen an Prozesseinheit oder Prozessmaschinen mit integriertem WIP/CIP (Wash in Place/Cleaning in Place), um Kontamination des Bedieners beim Öffnen einer staubigen Maschine zu verhindern, können ausreichend sein, um einen höheren Schutz zu gewährleisten.
Kontinuierliche Tablettenherstellung
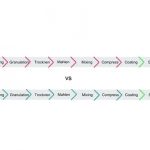
Einen neuen Trend stellt die kontinuierliche Tablettenherstellung dar, die Vorteile in der Produktionseffizienz, als auch im GMP-Footprint bedingt durch die geringere benötigte Fläche zum Aufstellen eines Prozesses in einer Fabrik beinhaltet. In diesem Herstellungsverfahren erfolgen alle Prozesse von der automatischen Einwaage, dem Granulieren, Trocknen, Vermischen von Bindemitteln, dem Tablettieren bis hin zum Coating in einem geschlossenen System im selben Raum bzw. in derselben Prozessanlage. Dies kann im Vergleich zu einer Batchherstellung bis zu 70 % des benötigten Produktionsraumes reduzieren. Zusätzlich bietet die kontinuierliche Tablettenherstellung die Möglichkeit, kontinuierliche Produktionsmaschinen für die Herstellung potenter Stoffe zu verwenden, bei der es keine manuellen Transfer- und Transportschritte des Produktes in einen Container zwischen den Prozessschritten gibt. Damit wird gleichzeitig auch die Gefährdung des Bedieners oder eine mögliche Kreuzkontamination mit anderen Produkten minimiert, da alle Prozessschritte geschlossen miteinander verbunden sind. Bild 3 zeigt einen Vergleich der Prozessabläufe bei einer klassischen Chargenproduktion (Batch) im Vergleich zur kontinuierlichen Herstellung (Konti). Prozessschritte, bei denen ein möglicher Kontakt mit potenten Stoffen möglich ist, sind rot markiert, Zwischenschritte, die inline und geschlossen sind, sind blau gekennzeichnet und ein sicheres Endprodukt ist grün markiert.
Fazit
Für die Handhabung hochaktiver Substanzen in der pharmazeutischen Herstellung ist es erforderlich, den Umfang des Containments richtig zu beurteilen und die Konsequenzen zu geringer Containment-Maßnahmen zu verstehen. Dafür müssen alle Faktoren, wie Potenz der produzierten Stoffe, Gebäudeanforderungen, Ventilation und vor allem Prozess und Prozessführung in die Sicherheitsbetrachtungen einbezogen werden. Zudem sollte das Containment-Konzept vorzugsweise eine höhere Sicherheitseinstufung berücksichtigen, als für das entsprechende Produkt erforderlich ist, um zukünftige Anpassungen zu erleichtern.
www.prozesstechnik-online.deSuchwort: php0316nnepharmaplan
Oliver Gottlieb
Principal Consultant,
Process Technology Consulting,
NNE Pharmaplan
Unsere Whitepaper-Empfehlung
Solida-Darreichungsformen: Vorteile und Grenzen verschiedener Batch-Granulier-Verfahren auf einen Blick. Treffen Sie mit dieser Entscheidungshilfe die richtige Wahl für Ihre Zielstellung.
Teilen: