Besonders die Entwicklung neuer Medikamente für Onkologie und Hormontherapie steigert den Bedarf an Containment-Lösungen. Bei der Verarbeitung dieser hochpotenten Substanzen steht der Schutz des Maschinenbedieners im Vordergrund. Gleichzeitig ist die Qualität des Endproduktes elementar – schließlich hängt die Gesundheit der Patienten davon ab. Doch wie viel Containment ist wirklich erforderlich? Und wie lässt es sich in der kostenintensiven Pharmabranche wirtschaftlich und vor allem flexibel umsetzen?
Auf den Grenzwert kommt es an
Auf der Wirkstoffseite lässt sich, ausgehend vom NOEL (No Observed Effect Level) und den erforderlichen Sicherheitsfaktoren, der Arbeitsplatzgrenzwert (OEL, Occupational Exposure Limit) in Mikrogramm pro Kubikmeter bestimmen. Der OEL ist die zeitlich gewichtete durchschnittliche Konzentration eines Stoffes in der Luft am Arbeitsplatz, bei der keine akute oder chronische Schädigung der Gesundheit der Beschäftigten zu erwarten ist. Bei der Festlegung wird von einer achtstündigen Exposition an fünf Tagen in der Woche während der Lebensarbeitszeit ausgegangen. Neben dem Arbeitsplatzgrenzwert hat sich zur Beschreibung der Toxizität aktiver Substanzen eine Einteilung in Bänder (OEB, Operational Exposure Band) mit aufsteigender Aktivität bewährt.
Ein risikobasierter Projektansatz
Sind der Wirkstoff und der OEL bekannt, sollten zwei weitere Faktoren für die Risikoanalyse berücksichtigt werden: der Verdünnungsgrad des Wirkstoffs und folglich die potenziell freigesetzte Wirkstoffkonzentration sowie die prinzipielle Neigung des Produkts, in die Luft zu gelangen, beispielsweise von trockenem Staub gegenüber nassem Granulat.
Neben der Charakterisierung des Wirkstoffs und seiner Eigenschaften ist es wichtig, das Leckagepotenzial der Produktionsanlage zu beschreiben. Hierzu wird für alle relevanten Komponenten der STTWA-Wert (Short Term Time Weighted Average) verwendet. Dieser kurzzeitgewichtete Mittelwert wird über
15 Minuten im Arbeitszyklus pro Equipment-Teil gemessen und gibt an, wieviel Produkt in µg/m3 als Leckage an die Umgebung abgegeben werden kann. Dabei wird davon ausgegangen, dass ein Bediener nur über die Atmung Wirkstoff aufnimmt und er pro Schicht 10 m3 Raumluft einatmet.
Bei der Risikoanalyse wird für jeden Prozessschritt, den der Bediener während seiner achtstündigen Arbeitszeit durchführt, die mögliche Exposition abgeschätzt und zum ROI-Gesamtwert (Real Operator Intake) summiert. Gleichzeitig ist über die Auswahl geeigneter Komponenten sicherzustellen, dass die Abschätzung der vom Bediener aufgenommenen Menge an Wirkstoff unterhalb des Grenzwertes liegt (Acceptional Daily Exposure, gemessen in µg/Tag).
Knackpunkte im Herstellungsprozess
Die meisten Anlagen operieren heutzutage mit einem geschlossenen Produktfluss. Geeignete dynamische und statische Dichtungen werden kontinuierlich überwacht und sorgen für optimale Sicherheit. Die Herausforderungen sind daher meist das Befüllen, die Probenahme und das Entleeren, da bei diesen Schritten das Produkt transferiert wird und auch freigesetzt werden kann. Um auch bei diesen Prozessschritten eine nach außen geschlossene Prozessführung zu gewährleisten, sind Doppelklappen die bevorzugte Lösung. Sie sind in unterschiedlichen Ausführungen verfügbar und liegen in Ihrem STTWA-Wert typischerweise deutlich unter 1 µg/m3.
Genauso wichtig – und häufig unterschätzt – sind Routine-Aufgaben wie Reinigung und Service. Hier muss verhindert werden, dass der Bediener eventuellen Produktrückständen an den Oberflächen der Anlage ausgesetzt wird. Moderne Anlagen verfügen daher über eine rezeptgesteuerte Reinigung mit hohem Automatisierungsgrad und einer minimierten Anzahl von Teilen, die manuell nachgereinigt werden müssen. Ob die Reinigungsdüsen für den Prozess korrekt platziert sind, kann dabei über einen Riboflavintest nachgewiesen werden. Vor der manuellen Nachreinigung müssen sämtliche Oberflächen, die mit dem Produkt in Kontakt kamen, sicher benetzt werden, um vorhandene Produktrückstände zu binden.
Hohe Effizienz bei geringem Risiko
Bei der Wahl des geeigneten Equipments steht neben der Sicherheit vor allem die effiziente und flexible Produktion im Vordergrund. Wer hier auf bewährte und markterprobte Technologien setzt, die bereits unter dem Wirtschaftlichkeitsfaktor entwickelt wurden, ist klar im Vorteil. Beispielsweise stattet Bosch Packaging Technology seine High-Shear-Mischer mit dem patentierten Mischwerkzeug Gentlewing aus. Die spezielle Form des gerundeten, Z-förmigen Rührers sorgt für eine besonders gründliche Entleerung des Produktbehälters. Das geringe Spaltmaß zwischen Behälter und Rührer minimiert darüber hinaus Produktanhaftungen an der Behälterwand und sorgt so für einen hohen Ertrag ohne manuelles Eingreifen.
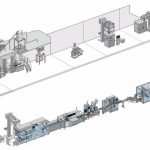
Zusätzliche Sicherheit entsteht durch die Überwachung des Produktflusses in der Anlage. So lässt sich beispielsweise eine drohende Blockade des Produkttransfers vom High-Shear-Mischer in die Wirbelschicht vorzeitig erkennen und durch Anpassung der Transferparameter verhindern. Für den Tierarzneimittelhersteller Vétoquinol hat Bosch Packaging Technology beispielsweise eine Anlage entwickelt, die aus einem High-Shear-Mischer mit Gentlewing, einer Wirbelschichtanlage sowie einem Kreislauf-Reinigungssystem besteht. Der gesamte Produktionsprozess findet in einem auf Doppelklappen basierenden Containment-System statt.
Der Weg zum sicheren Containment
Die Stärke eines erfahrenen Herstellers liegt darin, dass er ein Baukastensystem mit unterschiedlichen technischen Lösungen anbieten kann. Je nach Rahmenbedingungen und Ergebnis der ROI-Abschätzung können die einzelnen Komponenten gemeinsam mit dem Kunden zu einer Anlage kombiniert werden, die die Containment-Anforderungen mit ausreichender Sicherheit auch unter wirtschaftlichen Gesichtspunkten erfüllt. Die persönliche Schutzausrüstung (PPA) der Anlagenbediener sollte nur als allerletztes Mittel in Betracht gezogen werden.
Zum Abschluss der Containment-Bewertung kann während der Inbetriebnahme ein Smepac-Test durchgeführt werden, der den kompletten Batchverlauf von der Befüllung der Granulierlinie bis zum Entleeren in einen IBC bewertet. Der ISPE Good Practice Guide „Assessing the Particulate Containment Performance of Pharmaceutical Equipment” definiert die entsprechenden Rahmenbedingungen hierfür. Im Beispiel von Vétoquinol lieferte der Smepac-Test die erwarteten Ergebnisse: Die Messwerte aller Equipment-Teile lagen deutlich unter den geforderten Grenzwerten.
Diese Containment-Systematik lässt sich je nach Kundenanforderungen um weitere Komponenten wie Isolatoren, Tablettenpressen, Kapselfüller oder Trommelcoater variabel erweitern. Kombiniert mit der entsprechenden Erfahrung sowie Dokumentations- und Validierungsexpertise steht einem sicheren, flexiblen und effizienten Containment-Projekt nichts mehr im Weg.
Bosch Packaging Technology GmbH, Waiblingen