Formelzeichen: iS, Einheit: A/dm2.
Normierung der Stromstärke auf die Fläche, innerhalb derer der elektrischer Strom durchtritt.
Die Stromdichte gibt an, wie dicht die Elektronen in einem Leiter zusammengedrängt sind. Je dichter und je mehr Elektronen zusammenkommen, desto häufiger und heftiger stoßen die Elektronen gegen die Atome. Die Zusammenstöße setzen Wärmeenergie frei. Die Erwärmung des Leiters steigt.
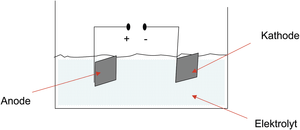
Beim elektrochemischen Polieren als angewandte Elektrolyse von Bauteilen z. B. aus austenitischen Edelstahllegierungen ist der Bauteil als Anode geschaltet, welchem eine Kathode als Werkzeug gegenüberliegt, wobei sich unter Zuhilfenahme einer externen Gleichstromquelle zwischen Anode und Kathode im Polierelektrolyten (Elektrolyt) ein elektrisches Feld aufbaut. Der Gesamtstrom fließt zwischen Kathodenfläche und Anodenfläche. Dividiert man den Gesamtstrom durch die strombeaufschlagte Anodenfläche, erhält man die anodische Stromdichte IS,a und entsprechend die kathodische Stromdichte IS,k durch Division des Gesamtstroms durch die Kathodenfläche.
Beide Stromdichten sind je nach konstruktiver Gegebenheit identisch oder aber verschieden. Die kathodische Stromdichte bestimmt letztlich die Kathodenbelegung. Die anodische Stromdichte bestimmt den prozessbedingten elektrochemischen Abtrag in Zeitfunktion, wobei sich der geometrische Abtrag aus dem elektrischen Ladungstransport und dem elektrochemischen Äquivalent errechnen lässt.
Grundsätzlich ist bei der Kathodenauslegung darauf zu achten, dass die elektrochemisch zu polierende Anodenfläche eine möglichst gleichmäßige Stromdichteverteilung aufweist, um einen gleichmäßigen Elektropolierabtrag am Bauteil sicherzustellen.
Abb. S 23: Schematische Darstellung eines Elektropolierprozesses in einem Elektrolyten. (Quelle: G. Henkel)
© 2013 – ECV – Lexikon der Pharmatechnologie