Bei der Entwicklung pharmazeutischer Produkte spielen Primärpackmittel eine
bedeutende Rolle: Sie werden als Bestandteil des Arzneimittels gesehen und unterliegen deshalb besonderen Anforderungen. Denn neben dem Wirkstoff und der Formulierung beeinflusst auch die Verpackung die Qualität, Wirksamkeit und Unbedenklichkeit
eines Arzneimittels. Hersteller müssen etwa bei der Zulassung eines neuen Medikaments nachweisen, dass die verwendeten Verpackungsmaterialien keine toxikologisch relevanten Substanzen wie etwa Bisphenol A, Kanzerogene oder mutagene Substanzen in die Formulierung abgeben.
Geregelt wird dies über zahlreiche Regularien, die genauso vielfältig sind wie die Verpackungen selbst. So bietet es sich für Hersteller an, bei der Wahl und Produktion der Primärverpackung mit einem erfahrenen Partner zusammenzuarbeiten, der in der Lage ist, sichere Lösungen zu entwickeln. Dazu gehört das Bensheimer Unternehmen Sanner, das seinen Schwerpunkt auf die Entwicklung und Produktion hochwertiger Kunststoffverpackungen gelegt hat. Im Bereich Regulatory Affairs stellt es sicher, dass alle verwendeten Materialien die Regularien erfüllen, die erforderlichen Grenzwerte eingehalten werden und dies durchgängig dokumentiert ist.
Arzneimittel und Medizinprodukte
Um die zutreffenden Regularien zu bestimmen, ist zunächst eine Unterscheidung
zwischen Arzneimittel und Medizinprodukt wichtig. Im Gegensatz zu Arzneimitteln, die pharmakologisch, immunologisch oder metabolisch wirken, erreichen Medizinprodukte ihre bestimmungsgemäße Hauptwirkung primär auf physikalischem Weg. Sie kommen typischerweise zur Anwendung, wenn Arzneimittel allein den gewünschten Effekt nicht erzielen können. Dazu gehören neben Herzschrittmachern auch Implantate, Produkte zur Injektion oder Transfusion sowie humanmedizinische Instrumente, Dentalprodukte und Labordiagnostika. Darüber hinaus gibt es auch Kombinationen aus Arzneimitteln und Medizinprodukten, beispielsweise Inhala-
toren für Asthma-Patienten oder Adrenalin-Injektoren für die Behandlung von Anaphylaxie. Entsprechend ihrer Verabreichung und Wirkung unterliegen sie anderen Regularien als klassische Arzneimittel.
Richtungsweisende Regeln
Weltweit sammeln Pharmakopöen anerkannte pharmazeutische Regeln über die Qualität, Prüfung, Lagerung und Bezeichnung von Arzneimitteln und die bei ihrer Herstellung und Prüfung verwendeten Stoffe, Materialien und Methoden. Besondere Relevanz haben die U.S. Pharmacopoeial Convention (USP) sowie die European
Pharmacopoeia (Ph.Eur.). Diese beinhalten beispielsweise spezielle Testmethoden für Kunststoffe und Trockenmittel.
Für die Entwicklung von Primärpackmitteln aus Kunststoff gibt es eine spezielle europä-ische Richtlinie (CPMP/QWP/4359/03), die zwischen festen und flüssigen sowie zwischen oralen, topischen, ophthalmischen, inhalativen und parenteralen Darreichungsformen von Arzneimitteln unterscheidet. Je nach Darreichungsform sind
bestimmte Angaben oder Tests erforderlich. Insbesondere bei nicht-festen Darreichungsformen für parenterale oder inhalative Anwendungen sind die Prüfanforderungen der Arzneibücher sehr umfangreich und streng. Die USP stellt darüber hinaus noch zusätz-liche Anforderungen an die biologische
Reaktivität von polymeren Primärpackmittelkomponenten.
Gerade in der Pharmabranche ist die Pflege und Aufrechterhaltung der Drug Maser Files (DMF) besonders wichtig. Dabei geht es um ein bei der amerikanischen FDA eingereichtes Schriftstück, in dem die pharmazeutische Herstellung und Qualitätssicherung von Arzneistoffen zum Zwecke der Arzneimittelzulassung dokumentiert werden. In einem DMF Type III können vertrauliche
Informationen speziell für Primärpackmittel hinterlegt werden. Nach Ausstellung des Letter of Authorization (LoA) durch den DMF-Inhaber hat die FDA als Drittpartei die Möglichkeit, diesen einzusehen und den entsprechenden Inhalt zu prüfen.
Die Erstellung eines DMF ist zwar nicht
gesetzlich verpflichtend, für weltweit agierende Unternehmen aber relevant, wenn sie ein Produkt in den USA zulassen wollen. Die Erstellung ist sehr aufwendig. Ihr Hauptzweck besteht darin, geistiges Eigentum, etwa in Bezug auf das Herstellungsverfahren, zugunsten des DMF-Inhabers zu schützen. So sollten sich Hersteller von Primärpackmitteln nicht nur mit dem Thema DMF auskennen, sondern auch alle für die Verpackung von Arzneimitteln relevanten Standardprodukte, die in den USA registriert werden sollen, in DMFs Typ III bei der FDA hinterlegen und regelmäßig aktualisieren.
Regulatory Affairs am Beispiel MDI
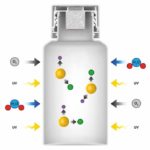
Die ganze Komplexität der für Primärverpackungen zu berücksichtigenden Regularien lässt sich gut an einem Beispiel illustrieren: Ein Dosieraerosol-Inhalator (MDI) ist eine Vorrichtung zur Abgabe von Medizin direkt in die Lunge. Er besteht aus einer unter Druck stehenden Kartusche, die eine Lösung oder Suspension des Wirkstoffes enthält. Freigesetzt wird der Wirkstoff durch ein Treibgas. Die Kartusche ist in einem Kunststoffgehäuse verankert, das wiederum mit einem Mundstück verbunden ist. Wenn die Kartusche nach unten gedrückt wird, gibt ein Ventil eine festgelegte Dosis des Wirkstoffes in einem definierten feinen Nebel ab. Dieser wird über das Mundstück in die Lunge inhaliert.
Aus regulatorischer Sicht muss bei einem MDI-Inhalator unterschieden werden, ob dieser für die einmalige Verwendung vormontiert angeboten wird, oder ob die Kunststoffhalterung der Kartusche, die das Arzneimittel enthält, beigepackt ist. Im ersten Fall handelt es sich um eine fixe Kombination Arzneimittel/Medizinprodukt, die nach den Vorgaben der neuen Medizinprodukteverordnung 2017/745 als Arzneimittel betrachtet wird. Tatsächlich ist der Begriff Kombinationsprodukt in der EU nicht rechtlich definiert. Hier wird unterschieden zwischen einem Medizinprodukt, das einen ergänzenden Stoff enthält und einem Produkt, das dazu bestimmt ist, ein Arzneimittel abzugeben.
Mehr als nur Verpackung
Beim MDI wird die Beurteilung im Rahmen der Arzneimittelzulassung durchgeführt.
Das impliziert, dass alle Testergebnisse nach ISO 10993 in der Zulassungsdokumentation vorliegen müssen, um die biologische Verträglichkeit der eingesetzten Materialien mit dem Körper zu bewerten. Somit werden nicht nur Produkte, sondern auch Ausgangsstoffe zur Herstellung von Medizinprodukten und Arzneimitteln untersucht. Auch die amerikanischen und europäischen Pharmakopöen kommen zum Tragen. Bei Primärpackmitteln für parenterale und inhalative Zubereitungen sollten zudem ausschließlich Materialien der strengsten Kompatibilitäts-Klasse laut USP eingesetzt werden.
Dieses Beispiel zeigt eindrücklich, welcher Aufwand sich hinter der Zulassung eines Pharmazeutikums verbergen kann. Es reicht längst nicht mehr aus, die im Arzneimittel selbst enthaltenen Stoffe genau zu prüfen und ihre Konformität zu belegen. Der Primärverpackung kommt eine immer wichtigere Rolle zu, denn sie hat einen nicht zu unterschätzenden Einfluss auf Qualität,
Sicherheit, Kompatibilität und Funktion des Produktes. Umso wichtiger ist die Rolle von Regulatory Affairs beim Primärpackmittelhersteller. Eine laufende Aktualisierung der benötigten DMF sollte genauso selbstverständlich sein wie die Beratung hinsichtlich Regulatory Affairs von Beginn einer Verpackungsentwicklung an.
Sanner GmbH, Bensheim