Seit dem 8. Oktober 2006 ist in Deutschland die erste Verordnung zur Herstellung von Arzneimittelwirkstoffen AMWHV verbindlich. Um ein GMP-Zertifikat für die Herstellung von Wirkstoffen zu erhalten, müssen die Vorgaben der Verordnung eingehalten und von den zuständigen Behörden geprüft werden. Dies bedeutet, dass Wirkstoffhersteller ihre Herstellbereiche entsprechend verifizieren und anpassen müssen, um Kreuzkontamination zu vermeiden und die Bediener in ausreichendem Maße zu schützen.
Richard Denk
Durch die Arzneimittelwirkstoffherstellverordnung (AMWHV) wurde die bereits seit Anfang 2006 in Kraft gesetzte Annex 18 des europäischen GMP-Leitfadens in nationales Recht umgesetzt. Folgender Wortlaut ist beispielweise in §5 (1) der AMWHV zu finden: „Die Betriebsräume müssen nach Art, Größe, Zahl und Ausrüstung für die beabsichtigten Zwecke geeignet sein und so ausgestattet und genutzt werden, dass das Risiko von Fehlern auf das kleinstmögliche Maß eingeschränkt und jeder die Qualität des Produktes beeinträchtigende Effekt vermieden wird.“ Dieser Paragraph bezieht sich in erster Linie auf die Vermeidung der Kreuzkontamination während der Herstellung von Zwischenstufen und auch der Endstufe. Insbesondere die Aussage, dass das Risiko von Fehlern auf das kleinstmögliche Maß eingeschränkt werden muss, ist sehr schwer zu greifen und abhängig vom herzustellenden Produkt. Bei der Herstellung von Paracetamol ist daher die Vermeidung der Kreuzkontamination sicherlich anders zu bewerten als bei der Hormonproduktion. So kann es bei der Herstellung von Paracetamol ausreichend sein, wenn der geschlossene Prozess in einem geeigneten Raum mit einem angepassten Containmentsystem zum Befüllen oder Entleeren in dafür vorgesehene Gebinde stattfindet. Wird dagegen ein Hormon hergestellt, sind neben einer geeigneten Raumtechnik auch Systeme zum Befüllen und Entleeren des Feststoffes vorzusehen, bei dem die Bediener in ausreichendem Maße geschützt werden. Bei einem offenen Produkthandling wiederum, müssen sich die Bediener Dekontaminationsprozeduren unterziehen, um zu vermeiden, dass es zu einer Kreuzkontamination über die Kleidung kommt. Von der FDA wird die Übertragung von Stoffen durch ungeeignete Schleusensysteme für die Mitarbeiter immer häufiger reklamiert. Diese Art der Kreuzkontamination ist seit langem bekannt und wird nun im Zuge der AMWHV geregelt. Hier wird auch das Wechseln und Verbleiben der Kleidung am Benutzungsort beschrieben.
Geschlossene Systeme
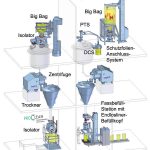
Für die Wirkstoffhersteller kommt durch die neue Verordnung einiges an Modernisierungs- und Anpassungsarbeit hinzu. Speziell beim Befüllen und Entleeren der Prozessbehälter wie Reaktoren, Zentrifugen und Trockner werden geschlossene Systeme zum Feststofftransfer verbindlich. In der Praxis erfordert dies geeignete geschlossene Systeme zur Handhabung von Zwischen- und Endprodukten gemäß einer toxikologischen Einstufung. Die Arbeitsplatzgrenzwerte variieren von kleiner 100 bis hin zu kleiner 10 µg/m³. Speziell bei CMR (Cancerogenic-Mutagenic-Reproduktionstoxisch)-Produkten wird ein Wert von bis zu kleiner 1 µg/m³ empfohlen oder gefordert. Für alle diese Anforderungen bietet Hecht unterschiedliche Containmentsysteme. Alle Systeme realisieren neben dem Personenschutz gleichzeitig auch den Produktschutz. In einem stets geschlossenen Prozess kann es zu keiner Kreuzkontamination kommen. Es ist nicht mehr zwingend notwendig, aufwendige Personen- und Materialschleusen zu integrieren um Kreuzkontamination zu vermeiden.
Die Schutzfoliensysteme verhindern Kontamination beim Wechsel eines Gebindes. Das prozessseitige Produktführungsrohr ist immer verschlossen und auch das Gebinde wird vor dem Entfernen von der Andockstelle mit einer Schutzfolie sicher verschlossen. Zu keinem Zeitpunkt gelangt Produkt in die Umgebung. Bei Gebinden mit genügend langem Inliner kann ein Teil des Inliners als Schutzfolie verwendet werden. So können vor allem Big Bags geschlossen befüllt und entleert werden. Für höchstes Containment (total Containment) werden Big Bags mit zwei Inlinern verwendet. Der äußere Liner wird außen an einem Isolator, der im kontinuierlichen Unterdruck (-50 bis -70 Pa) betrieben wird, fixiert. Erst nachdem die Dichtigkeit dieser Verbindung getestet wurde, wird der Isolator geöffnet und der innere Liner im Innern des Isolators mithilfe von Handschuhen angeschlossen.
Einsatz von Endloslinern
Als Beispiel eines geschlossenen Systems zur Entleerung einer Zentrifuge oder eines Trockners wird nachfolgend ein Endloslinersystem beschrieben. Durch Einsatz von Endloslinertechnologie kann ein Prozessapparat mit geringen Umbauarbeiten zu einer GMP-gerechten Ausführung werden und dadurch die Vorgaben der AMWHV erfüllen. An den Auslaufflansch einer Zentrifuge oder eines Trockners wird eine Aufnahmevorrichtung für 30 bis 50 m Folie adaptiert. Das Folienende wird am Anschlussadapter staubdicht befestigt, der Folienanfang von einer Folienkassette gezogen und mit einem Clip verschlossen oder verschweißt. Nachdem ausreichend Folie in ein Fass oder Karton gelangt ist, erfolgt das Befüllen des Liners mit Produkt. Oberhalb des Produkts wird der Liner zweimal in kurzem Abstand verschlossen und mittig zwischen den Verschlüssen getrennt. Bei Folienschweißen bildet eine Dreifachschweißnaht automatisch die Verschlussnaht, die Trennnaht und die neue Bodennaht. Mit diesem Prinzip wird sichergestellt, dass es zu keiner Zeit zu einer Kreuzkontamination kommen kann. Weiterhin dient dieses System auch als Personenschutz. Nachdem die Folie aufgebraucht ist, erfolgt ein kontaminationsfreier Folienwechseln. Auch eine geschlossene Reinigung des Systems ist möglich.
Bei der Planung und Inbetriebnahme einnes solchen Systems sollte auf jeden Fall ein Experte im Bereich Containment für Feststoffe (geschlossene Prozesse) mit einbezogen werden. Es kommt immer wieder vor, dass ein geschlossenes System in einen Prozess integriert wird und wichtige Punkte übersehen werden, da nicht der gesamte Prozess betrachtet wurde.
Halle 9, Stand 425
cav 434
Mehr zu den Produkten
AMWHV Arzneimittel- und Wirkstoffherstellungsverordnung
Powtech 2007
Unsere Webinar-Empfehlung
Die Websession „Wasserstoff in der Chemie – Anlagen, Komponenten, Dienstleistungen“ (hier als Webcast abrufbar) zeigt technische Lösungen auf, die die Herstellung und Handhabung von Wasserstoff in der chemischen Industrie sicher machen und wirtschaftlich gestalten.
Ob effizienter…
Teilen: