Die Erhöhung des Automatisierungsgrades bei gleichzeitiger Verbesserung der Qualität sind heute zwei treibende Themen in der pharmazeutischen Industrie. Aus diesem Grund werden von den Herstellern für die Produktionsprozesse immer häufiger die Funktionen elektronische Aufzeichnung und elektronische Unterschrift – wie in der FDA-Vorschrift 21 CFR Part 11 beschrieben – gefordert. Das Scada-System Simatic WinCC hilft bei der Erfüllung dieser Anforderungen.
Dipl.-Ing. Matthias Bruns, Dipl.-Ing. (FH) Karlheinz Büscher
Die amerikanische Gesundheitsbehörde FDA schreibt in der Good Manufacturing Practice (GMP) die Randbedingungen vor, unter denen pharmazeutische Produkte hergestellt werden müssen. Durch die Validierung einer Anlage stellt die FDA sicher, dass das Design und die Prozesse den Vorschriften entsprechen. Moderne Fertigungen sind heute hoch automatisiert. Damit liegen alle wesentlichen Informationen automatisch elektronisch vor. Im Wesentlichen beschreibt 21 CFR Part 11 die Anforderungen an den Einsatz von elektronischen Aufzeichnungen (electronic record) und elektronischen Unterschriften (electronic signature). Für ein Scada-System heißt dies konkret:
- Zugriffskontrolle und elektronische Unterschrift: Über die Zugriffskontrolle wird sichergestellt, dass nur autorisierte Benutzer Bedienungen an der Anlage vornehmen dürfen. Die elektronische Unterschrift ersetzt die manuelle Unterschrift und besitzt die gleiche Gültigkeit.
- Audit Trails und Change Control: Für Bedieneraktivitäten im Runtime-Betrieb wie auch für Änderungen an der Projektierung gilt, dass unverfälschbar aufgezeichnet werden muss, wer was wann geändert hat und warum.
- Archivierung und Lesen der Daten: Die so entstandenen Audit-Trail-Informationen müssen in einem Langzeitarchiv gespeichert und zu einem späteren Zeitpunkt wieder gelesen werden können.
Das Prozessvisualisierungssystem Simatic WinCC V6 gewährleistet den Zugriffsschutz für alle Komponenten im System, über die Veränderungen der Anlage vorgenommen werden können. Jeder Benutzer wird von WinCC einer Benutzergruppe zugeordnet, mit definierten Funktionsrechten am System. Damit wird verhindert, dass z. B. Wartungspersonal unerlaubt Rezepturen verändern oder starten kann.
Da die FDA vorschreibt, dass Handlungen innerhalb der Anlage eindeutig Personen zugeordnet werden müssen, protokolliert WinCC V6 in Kombination mit der Option Simatic-Logon-Service die Login- und Logout-Prozesse mit Zeitstempel im Audit Trail. Darüber hinaus erfüllt WinCC weitere Vorschriften, z. B. die Zwei-Komponenten-Autorisierung mit Benutzer-ID und Passwort, die Passwortalterung, damit regelmäßig Passwörter erneuert werden, das Sperren von Benutzern durch den Administrator und das automatische Logout bei längerer Inaktivität des Benutzers. Dies gilt sowohl für Stand-alone-Systeme als auch für komplexe Client-Server-Strukturen. Simatic Logon Service bietet auch eine Zugriffskontrolle via Chipcard an.
Elektronische Unterschrift
In GMP-relevanten Produktionsprozessen bestätigt die Unterschrift des Verantwortlichen im Chargen-Protokoll die ordnungsgemäße Herstellung einer Charge. Ebenso sind Rezeptparameteränderungen mit Unterschrift zu bestätigen, um damit die Verantwortung für das veränderte Endprodukt klar zu definieren. Gemäß 21 CFR Part 11 kann dieses Unterzeichnen auch elektronisch erfolgen, wenn vorher schriftlich fixiert wurde, dass die elektronische Unterschrift die gleiche Gültigkeit wie die manuelle Unterschrift besitzt. Die elektronische Unterschrift erfolgt analog zur Zugriffskontrolle durch Abfrage von Benutzer-ID und Passwort.
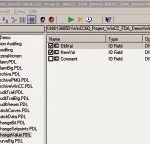
WinCC erfasst im Audit Trail die Bedieneraktivitäten während des Runtime-Betriebes. Der Anlagenbetreiber kann dabei festlegen, ob er alle Bedienobjekte oder ob er selektiv einzelne Objekte überwachen will. Einzelne Objekte können z. B. Parameter, Slider und E/A-Felder sein. Vorteil einer selektiven Vorgehensweise ist, dass der Audit Trail immer übersichtlich bleibt und nur die GMP-relevanten Objekte erfasst werden. Die Software zeichnet im Audit Trail Informationen wie Zeitstempel, Objektname, Bediener, Alt- und Neuwert, Aktionsbezeichnung und Kommentare auf. Über diese Standardfunktionen hinaus bietet WinCC die Funktion Audit Entry an, um individuelle Aktivitäten wie das Auslösen von Funktionsknöpfen, das Selektieren in einer Checkbox oder andere benutzerspezifische Bedienobjekte zu protokollieren.
Audit Trail für Projektierung
Auch im laufenden Betrieb einer validierten Anlage sind hin und wieder Änderungen in der Projektierung notwendig. Die Entscheidung über die Durchführung einer geplanten Änderung, die Bewertung ihrer Folgen und zusätzliche Maßnahmen wie z. B. Revalidierung obliegt den pharmazeutisch Verantwortlichen und wird durch ein Change Control unterstützt und dokumentiert. Generell kann man sagen, dass alle Veränderungen des zu produzierendenden Endproduktes zu einer Neuvalidierung führen. Letztendlich sind alle Veränderungen einer Anlage von Produktionsbeginn über die gesamte Lebensdauer zu erfassen. Dementsprechend ist die Projektierung, ähnlich dem Runtime-Betrieb, im Audit Trail der Projektierung zu protokollieren. Mit WinCC kann jegliche Art von Projektierungsänderungen erfasst werden. Damit werden die Anforderungen der Behörden zum Thema Change Control erfüllt. Zusätzlich sind die Änderungen im Runtime und in der Projektierung gleichzeitig in einer zeitlichen Reihenfolge zu sehen, was besonders bei der Analyse von fehlerhaften Chargen sehr vorteilhaft ist.
WinCC Audit unterscheidet zwischen Konfigurationsänderungen und der Dokumentenkontrolle. Unter Konfigurationsänderung werden Änderungen wie das Neuanlegen von Variablen und das Verändern von Alarmtexten und User-Daten verstanden. Dabei überwacht WinCC Audit die interne Datenbank von WinCC und protokolliert alle Änderungen automatisch und lückenlos mit.
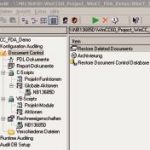
Die Dokumentenkontrolle umfasst Anlagenbilder, Skripte, Protokoll-Layouts und anwenderspezifische Dokumente. All diese Dokumente bzw. Dateien überwacht WinCC Audit auf Veränderungen. Die Software erzeugt von den Zwischenversionen der Dokumente binäre Files und legt sie in einer separaten SQL-Datenbank ab. Auf diese Weise kann immer wieder auf ältere Zwischenstände zugegriffen werden. Um die Dateien automatisch verwalten zu können, werden Funktionen wie Check in, Check out und Rollback angeboten. Damit kann jegliche Veränderung im Runtime-Betrieb, in der Projektierung oder in der Dokumentenkontrolle lückenlos nachverfolgt werden.
Lesen der Audit Trails
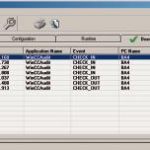
WinCC Audit bietet für die Analyse der Audit Trails einen Viewer mit vielfältigen Filter- und Selektiermöglichkeiten an. So lassen sich zum Beispiel folgende Daten im Audit Trail protokollieren: Ereignis/Funktion, Zeit und Datum der Änderung, Benutzername, Datenbankname, alter Wert/neuer Wert und Kommentar/Änderungsgrund. Auch diese Audit-Trail-Einträge legt WinCC als Datensätze in einer SQL-Datenbank ab und schützt sie so gegen Veränderung. Komfortabel kann diese Datenbank von WinCC Audit zentral oder dezentral – auf einen beliebigen Netzwerk-PC im Client/Server-Netz – organisiert werden. Die Datenbank kann über viele Jahre archiviert und auch noch nach dem Abschalten der Anlage verfügbar gehalten werden.
Damit werden alle zentralen Forderungen der FDA erfüllt. WinCC unterstützt somit Anlagenbetreiber, Systemintegratoren und Maschinenbauer bei der Implementierung und Validierung ihrer Anlagen gemäß 21 CFR Part 11, wobei die vollständige Erfüllung der Anforderungen aus dieser Vorschrift nur in Kombination mit Verfahrensanweisungen und organisatorischen Vorgaben erreicht werden kann.
cav 454
Guidance for Industry: Part 11, Electronic Records; Electronic Signatures – Scope and Application
Weitere Informationen zu WinCC V6
Unsere Webinar-Empfehlung
Die Websession „Wasserstoff in der Chemie – Anlagen, Komponenten, Dienstleistungen“ (hier als Webcast abrufbar) zeigt technische Lösungen auf, die die Herstellung und Handhabung von Wasserstoff in der chemischen Industrie sicher machen und wirtschaftlich gestalten.
Ob effizienter…
Teilen: