Arzneimittelhersteller stehen bei der Umsetzung von Richtlinien zum Schutz der Verbraucher und des Bedienpersonals vor einer doppelten Herausforderung: länderspezifisch abweichende Anforderungen und sich stetig wandelnde Gesetze. Die Zusammenarbeit mit Anlagenherstellern, die über Know-how und Erfahrung bei der Entwicklung und Einführung international ausgerichteter Lösungen verfügen, kann hier von Vorteil sein.
Autor Dirk Bettels Senior Product Manager, Mettler-Toledo Garvens
Eine Vielzahl unterschiedlicher Richtlinien und Normen werden in der Pharmaindustrie eingesetzt, um den Schutz der Endverbraucher und des Personals zu gewährleisten. Verbraucherschutzseitig fordert Richtlinie 2011/62/EU die Einführung von Serialisierungsprozessen, um so das Eindringen von Fälschungen in die legale Vertriebskette der EU-Mitgliedstaaten zu verhindern. Personalschutzseitig formulieren die europäische Norm EN 12100 und ihr amerikanisches Äquivalent Ansi B155-2011 allgemeine Leitsätze zur Beurteilung und Minderung von Risiken und unterstützen Konstrukteure bei der Herstellung von Maschinen, die sich sicher bedienen lassen. Die Umsetzung solcher Vorschriften erweist sich in der Praxis oft als tückisch, denn die jeweils gültigen Standards können von Land zu Land variieren. Während Arzneimittelverpackungen in den USA mit fortlaufenden Seriennummern versehen werden, hat die Auswahl in Europa nach dem Zufallsprinzip zu erfolgen; maschinelle Schutzmaßnahmen, die in Amerika Pflicht sind, gelten nicht notwendigerweise auch in China.
Serialisieren über alle Fertigungsstufen
Um in Sachen Verbraucherschutz auf der sicheren Seite zu sein, sollten Medikamentenhersteller Maschinen nutzen, die den aktuellen Richtlinien der Zielmärkte entsprechen – und sich bei Bedarf flexibel an zukünftige Standards anpassen lassen. Ein aktuelles Beispiel für diese Notwendigkeit stellt die 2011 vom Europäischen Parlament erlassene Arzneimittelfälschungsrichtlinie 2011/62/EU dar, die alle EU-Mitgliedstaaten bis 2017 verpflichtet, Medikamente zu serialisieren, sprich: diese mit Sicherheitsmerkmalen zu versehen, die das eindeutige Prüfen und Nachverfolgen über alle Fertigungsstufen hinweg ermöglichen.
Zu den Sicherheitsmerkmalen zählen neben Tamper-Evidence-Verfahren, die die Unversehrtheit der Originalverpackung garantieren, auch Kennzeichnungsmethoden wie 2-D-Barcodes. Für deren Umsetzung benötigen Medikamentenhersteller technische Lösungen zur Erzeugung randomisierter Seriennummern sowie Druck- und Kamerasysteme zur Erstellung und Verifizierung. Die jeweiligen ländertypischen Anforderungen lassen sich dabei nur mit automatisierten elektronischen Systemen berücksichtigen, die zudem auch in der Lage sind, ein Datenmanagement aufrechtzuerhalten, das über alle Fertigungsstufen hinweg sicher und zuverlässig arbeitet. Durchgängige Serialisierungslösungen decken von der Erfassung der einzelnen Faltschachtel bis zur Aggregation der Einzeleinheiten auf Paletten sämtliche Bereiche des Verpackungsprozesses ab. Außerdem stellen sie sicher, dass mehrere Produktionslinien standortübergreifend an eine zentrale Datenbank angeschlossen werden können, die später als Basis für die Anfertigung der vorgeschriebenen Reports dient.
Führende Anbieter von Serialisierungssystemen wie Mettler-Toledo unterstützen Arzneimittelhersteller durch skalierbare Lösungen, die sich passgenau an die jeweils vorherrschenden Bedingungen anpassen. So eignet sich das Stand-Alone-System XMV mit integriertem Inkjet-Drucker und Kontrollkamera ideal für Unternehmen, die bereits über eine Kontrollwaage verfügen und ihre Produktionslinie gezielt um eine Serialisierungslösung erweitern wollen. Einen Schritt weiter gehen Komplettlösungen wie XS2 MV, die Wägen, Kennzeichnen und Verifizieren kombinieren, oder XS2 MV TE, das darüber hinaus mit einem Tamper-Evidence-Modul ausgestattet ist. Gemein ist den genannten Systemen, dass sie internationalen Vorgaben zur Sicherung von Pharmaprodukten gegen Fälschungen entsprechen und somit in allen Zielmärkten eingesetzt werden können.
Detaillierte Gefahrenanalyse
Bei der Produktion von Maschinen, die in puncto Bedienschutz allen relevanten Auflagen genügen, hat es sich bewährt, sicherheitstechnische Aspekte an den Anfang des Konstruktionsprozesses zu stellen. Auf diese Weise lassen sich potenzielle Gefahrenstellen antizipieren und durch Modifikationen im Design oder durch abfedernde Gegenmaßnahmen sofort beheben. Die Intention besteht nicht darin, eine zu hundert Prozent sichere Anlage zu entwickeln. Das ist bei Systemen, zu denen Personen Zutritt haben, erstens schlicht unmöglich und zweitens würde bereits der Versuch die Maschine unbedienbar werden lassen. Vielmehr geht es darum, das Risiko für das Personal angemessen zu reduzieren – und sich für eine universelle Nutzbarkeit des Systems dabei stets am striktesten Standard zu orientieren. Als Hersteller von Produktinspektionslösungen setzt Mettler-Toledo auf ein mehrköpfiges Team aus Entwicklern, Sicherheitsbeauftragten, Konstrukteuren sowie Qualitäts- und Produktmanagern, das alle maschinellen Komponenten noch in der Planungsphase einer detaillierten Gefahrenanalyse unterzieht. Die heterogene Ausrichtung der Arbeitsgruppe stellt sicher, dass bei der Konstruktion der Systeme sicherheitstechnische Standards wie EN 12100 und Ansi B155-2011 berücksichtigt und mit weiteren relevanten Aspekten, wie der Ergonomie oder Markttauglichkeit, in Einklang gebracht werden.
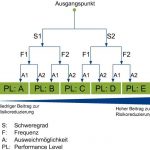
Zu Beginn der Gefahrenanalyse werden generelle Fragen zu den einzelnen Maschinenmodulen, beispielsweise zum Förderband, und deren einzelnen Elementen, etwa zum Zahnriemen, beantwortet: In welchem Bereich wird der Gegenstand eingesetzt? Welche Gefahr geht von ihm aus? Kommt geschultes oder ungeschultes Personal mit ihm in Kontakt? In welcher Phase tritt die Gefahr auf – während der Montage, des Betriebs oder des Recyclings? Anschließend wird der Performance Level (Bild 2) jeder Komponente durch die Verrechnung folgender Faktoren ermittelt:
- Schweregrad: Welchen Schaden kann die Gefahr verursachen – eine Schramme oder abgetrennte Körpergliedmaße?
- Frequenz: Wie oft und wie lange setzt sich das Bedienpersonal der Gefahr aus – wird das System automatisch oder manuell gesteuert?
- Ausweichmöglichkeit: Welche Chance besteht, der Gefahr auszuweichen – bewegt sich die gefährliche Komponente langsam oder schnell?
Der Performance Level des Elements determiniert im weiteren Entwicklungsprozess, wie etwa die Elektrik der Komponente auszulegen ist. Wird für einen Anlagenbereich der Performance Level D identifiziert, wissen die verantwortlichen Mitarbeiter zum Beispiel, dass sie einen qualitativ hochwertigen Notausschalter einbauen müssen und wählen statt des einfachen Öffner- und Schließer-Kontakts eher die zweikanalige Variante mit Software-gesteuerter Selbstüberwachung. Auch der Sicherheitsschaltkreis – die Aktionen, die eingeleitet werden, wenn der Notausschalter betätigt wird – wird wie von EN ISO 13849 gefordert nach dem festgestellten Performance Level gestaltet.
International ausgerichtete Anbieter
Für eine universale Einsetzbarkeit müssen Produktionssysteme die Verbraucherschutzrichtlinien der relevanten Zielmärkte erfüllen und über ein Design verfügen, das die Sicherheit des Personals optimal gewährleistet. Aus diesem Grund sind gerade international agierende Medikamentenhersteller gut beraten, die Aspekte Verbraucher- und Bedienschutz bei der Anschaffung ihrer Anlagen zu berücksichtigen – und auf Maschinenlieferanten zu setzen, die über das technologische Know-how und die langjährige Erfahrung bei der Entwicklung und Einführung international ausgerichteter Lösungen verfügen.
prozesstechnik-online.de/cav1214404
Unsere Webinar-Empfehlung
Lebensmittel müssen sicher sein! Im Rahmen der Websession Lebensmittelsicherheit stellen sechs Referent:innen neue Ansätze und Lösungen vor, die beim Erreichen dieses Ziels helfen.
Teilen: