Bedienen sich Life-Sciences-Unternehmen computergestützter Systeme, etwa zum Monitoring von Klima- und Prozessmessdaten, müssen sie während des gesamten Systemlebenszyklus dessen Konformität und dessen Eignung für den vorgesehenen Zweck sicherstellen. Die risikoorientierte Spezifizierung, die Umsetzung (Inbetriebnahme) sowie die nachfolgende Verifizierung – unter den beiden genannten Aspekten der Konformität und der Eignung – sind dabei gleichbedeutend mit der Validierung des Systems.
Autor Jens Amberg , Geschäftsbereichsleiter, Testo Industrial Services
Stand der Technik für solche Computer-Software-Validierungen (CSV) ist heute der Leitfaden GAMP 5, der von der ISPE herausgegeben wird. Letztlich muss der jeweilige pharmazeutische Anlagenbetreiber entscheiden, ob er diesen Leitfaden zugrunde legt oder nicht; die Erfüllung der Regulatorien liegt in seiner Verantwortung.
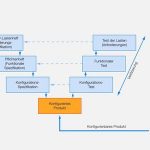
Auch Monitoringsysteme unterliegen der Validierungspflicht. Bei diesen Systemen handelt es sich um Messdaten-Erfassungssysteme, die über ein hohes Maß an Datensicherheit verfügen, um qualitätsrelevante Messdaten sicher zu erfassen, zu übertragen und zu speichern. Bei Grenzwertüberschreitungen werden Alarme abgesetzt, damit der Betreiber ungewollte Zustände unmittelbar beseitigen kann. Im Folgenden wird exemplarisch die Validierung des Monitoringsystems Testo Saveris CFR nach GAMP 5 vertieft (Bild 1).
Berücksichtigung von GAMP 5
Zu den kritischen Einflussfaktoren für die Sicherheit pharmazeutischer Herstellung zählt das Produktions- und Lagerklima. Darüber hinaus sind in der Regel zahlreiche unmittelbare Prozessparameter relevant für den Pharmazeuten, so etwa Temperaturen in Brutschränken oder in Kühlräumen. Solche und andere Messdaten werden heute zunehmend automatisiert in Monitoring-Systemen erfasst, nachdem sie über viele Jahre über eine Messgeräte-Handablesung oder manuelle Datenlogger-Auslesungen erhoben wurden.
Diesem Trend entspricht das Monitoring-System Saveris CFR, das Funk- und Ethernetfühler mit dezentralen Speichern zur Verfügung stellt, die ihre Daten an eine Basisstation weiterreichen. Diese ist auch ohne PC-Bereitschaft in der Lage, über Relais oder SMS Alarme abzusetzen sowie große Datenmengen zu speichern. Somit ist mehrstufig dafür gesorgt, dass höchste Datensicherheit und -integrität gewährleistet bleibt. Abgerundet wird das System durch eine netzwerkfähige Software mit SQL-Datenbank, die manipulationssicher die Daten darstellt, PDF-Berichte generiert und in der Lage ist, via E-Mail zu alarmieren.
Da es sich bei dieser Anwendung um eine automatische, elektronische Datenerhebung und -speicherung handelt, greifen die Bestimmungen nach 21 CFR part 11, der FDA-Vorschrift zur Sicherstellung manipulationsgeschützter Datenaufzeichnung. Diese Anforderungen, wie
- Audit Trail mit Historie aller relevanten Vorkommnisse und Parametrierungen
- elektronische Signatur (Passwort-geschützte Interaktionen)
- Zugangsschutz zu kritischen Software-Funktionen
- Nutzer-Berechtigungskonzept
werden bei dem Monitoringsystem Saveris CFR erfüllt, wie seitens des Fraunhofer-Instituts IESE bestätigt wurde.
Die meisten GxP-regulierten Hersteller werden sich bei der Entscheidung für ein Messdaten-Monitoring-System daran orientieren, ob seitens des Lieferanten zugleich eine Validierung – unter Berücksichtigung von GAMP 5 – unterstützt wird, um gegenüber Inspektoren der regulierenden Behörden eine sichere Position einnehmen zu können.
Ablauf einer Validierung
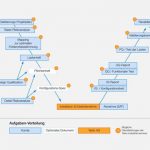
Mit dem Ziel einer angepassten Skalierung der jeweiligen Validierung unterscheidet GAMP 5 verschiedene Kategorien von computergestützten Systemen. Testo Saveris fällt hierbei unter die Kategorie 4 (konfigurierbares Produkt). Das Vorgehen bei dieser Kategorie wird in Bild 2 dargestellt. Es wird erkennbar, dass Spezifizierung und Verifizierung schwerpunktmäßig Aufgaben des regulierten Unternehmens sind, während die Produktkonfigurierung (hier: die Inbetriebnahme des Systems) in eindeutiger Lieferanten-Verantwortung liegt.
In vielen Fällen ist es für das regulierte Unternehmen aber wünschenswert, bei der Validierung professionelle externe Unterstützung zu erhalten. So wird (übrigens weltweit) im Rahmen der Validierung des Systems Saveris CFR auf die Dienstleistungen von Testo Industrial Services zurückgegriffen, wodurch klare Vorteile erzielt werden können:
- fachkundige Unterstützung aufgrund der Saveris-Systemkenntnis sowie langjähriger Validierungspraxis im Pharma-Umfeld
- Bewältigung betreiberinterner Personalengpässe, speziell bei zeitgleicher Validierung umfangreicher Neuanlagen
- alle Leistungen aus einer Hand bedeutet weniger Schnittstellen
- kein Einarbeiten des Validierungs-Dienstleisters am Kundenprojekt
Wie Bild 3 zeigt, kann dabei die Leistungstiefe der unterstützenden Dienstleistungen passend zugeschnitten werden. So kann der Betreiber ganz individuelle Unterstützung erhalten und sich auf sein Kerngeschäft konzentrieren, ohne auf eine professionelle Validierung verzichten zu müssen, die der Tatsache gerecht wird, dass Monitoring-Systeme beliebte Fragefelder pharmazeutischer Audits darstellen.
GAMP 5 schreibt dabei der Betreiberfirma nicht vor, alle o.g. Schritte zwingend durchzuführen oder exakt so zu benennen. Ebenso werden die Bezeichnungen IQ, OQ, PQ zwar im GAMP 5 nicht weiter verwendet, den Firmen wird aber freigestellt, sich nach wie vor dieser eingeführten Terminologie zu bedienen. Was die Wahl der Schritte angeht, so wird, analog zu ASTM E2500, dem US-amerikanischen Ansatz pharmazeutischer Validierungen, lediglich gefordert, dass den „angemessenen“ Spezifikations-Aktivitäten entsprechende Verifikationsschritte folgen müssen, in denen die Einhaltung der Spezifikation überprüft wird. Vergleicht man diese Grundhaltung mit den deutlich starreren Forderungen früherer Leitfäden wie dem GAMP 4, so wurde mit GAMP 5 ein großer Schritt getan in Richtung einer nicht nur sicheren – weil konsequent risikobasierten –, sondern auch wirtschaftlich vertretbaren Validierung.
Online-Info www.pharmaproduktion.com/0110456
Unsere Webinar-Empfehlung
Der Webcast MTP und modulare Produktion bietet eine einzigartige Gelegenheit, mehr über die aktuellen Entwicklungen bei MTP und in der modularen Produktion zu erfahren.
Chemie- und Pharmaproduktion braucht mehr Flexibilität
In der heutigen sich schnell wandelnden Welt stehen…
Teilen: